Часть 11 раздела 21 Свода федеральных нормативных актов США (CFR) определяет критерии в отношении целостности электронных данных, установленные Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA). Подотчетные FDA промышленные предприятия, такие как производители медицинских устройств и фармацевтические компании, должны соблюдать правила части 11 раздела 21 CFR для обеспечения точного ведения электронных записей и подписей.
Однако, чтобы соблюсти все требования, может потребоваться немало усилий и времени. В этом выпуске блога мы рассмотрим сложности, связанные с соблюдением правил части 11 раздела 21 CFR, и обсудим, как можно их преодолеть.
Сложности, связанные с соблюдением правил части 11 раздела 21 CFR
Обеспечение соответствия обычно подразумевает создание рабочих инструкций для соблюдения каждого отдельного правила части 11 раздела 21 CFR, разработку протоколов валидации для обеспечения правильной настройки, эксплуатации и производительности оборудования и программного обеспечения, создание стандартных операционных процедур (СОП) и интенсивное обучение персонала по работе с оборудованием и программным обеспечением.
Любой инструмент, который способен упростить все эти процедуры, будет полезен.
Многие подотчетные FDA промышленные предприятия используют нашу систему контроля промышленной чистоты OLYMPUS CIX100. Система CIX100, оснащенная интуитивно понятным интерфейсом, технологией эффективного сбора данных и функциями для ускоренного создания отчетов, поможет вам легко и быстро оценить чистоту готовых изделий для определения их соответствия корпоративным и международным стандартам.
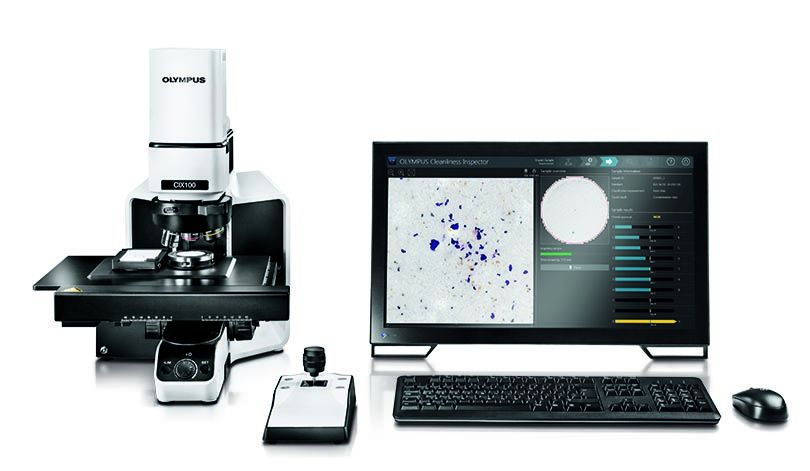
Система контроля промышленной чистоты OLYMPUS CIX100.
Чтобы помочь вам в обеспечении соответствия всем необходимым требованиям, мы создали пакет 21 CFR Part 11 для системы контроля промышленной чистоты CIX100.
Соответствие правилам части 11 раздела 21 CFR — с системой контроля промышленной чистоты CIX100 просто, как никогда
Пакет CIX100 21 CFR Part 11 демонстрирует, как система CIX100 может обеспечивать соответствие каждому требованию, и предоставляет инструкции по настройке и эксплуатации системы. При правильной интеграции пакета все данные, получаемые системой CIX100, будут соответствовать требованиям CFR (Часть 11, Раздел 21).
Пакет включает в себя:
- Подробное описание того, как система CIX100 со службой Adobe Sign обеспечивает соответствие конкретным требованиям части 11 раздела 21 CFR
- Протокол валидации для квалификации монтажа/функционирования (IQ/OQ) системы CIX100
- Стандартная операционная процедура (СОП) для системы CIX100 в соответствии с правилами части 11 раздела 21 CFR
- Рабочие инструкции по установке и эксплуатации системы CIX100 в соответствии с правилами части 11 раздела 21 CFR
Общий план по обеспечению соответствия правилам части 11 раздела 21 CFR
В этих подробных указаниях вы найдете все, что вам нужно знать для полного соответствия требованиям части 11 раздела 21 CFR. Там же описаны предлагаемые нами решения и действия, необходимые со стороны пользователя. Краткий обзор предоставляемой информации
Решения Olympus для обеспечения соответствия правилам части 11 раздела 21 CFR:
- Валидация системы для получения точных и достоверных результатов при проведении IQ/OQ
- Обучение пользователей по правильной эксплуатации системы CIX100
- Обеспечение надлежащего функционирования системы посредством предоставления подробных СОП
- Ограничение доступа к системе только для правомочных пользователей посредством защищенного входа в систему через ПК Windows и управления правами пользователей
- Использование службы Adobe Sign для хранения электронных подписей и отслеживания PDF отчетов с результатами контроля образцов
Обязательные действия со стороны пользователей:
- Обучение использованию Adobe Sign для хранения электронных подписей и отслеживания электронных данных
- Создание политик по использованию ПО CIX100 с Adobe Sign, а также по отслеживанию доступов и пересмотров предыдущих отчетов с результатами контроля образцов
- Соблюдение процедур по управлению убытками и хранению документации
С помощью этого пакета система CIX100 поможет оптимизировать процедуры контроля чистоты и обеспечить соответствие стандартам FDA в отношении электронных записей и подписей.
См. также
Введение в контроль промышленной чистоты
Брошюра: Стандарты промышленной чистоты
Связаться с нами

